Prescrições Médicas
Índice
Informações Gerais sobre Prescrições[editar]
De acordo com a Política Nacional de Medicamentos Portaria GM n° 3.916/98, a prescrição é o ato de definir o medicamento a ser consumido pelo paciente, com a respectiva dosagem e duração do tratamento; esse ato é expresso mediante a elaboração de uma receita médica. A prescrição é o instrumento no qual se apoia a dispensação. Deve cumprir os aspectos legais contidos na Lei n. 5991/73. O Art. 35 dessa lei estabelece que a receita deverá ser aviada se:
a) estiver escrita a tinta, em vernáculo por extenso e de modo legível, observados a nomenclatura e sistema de pesos e medidas;
b) contiver nome e endereço residencial do paciente;
c) contiver descrito o modo de usar o medicamento;
d) contiver a data e assinatura do profissional, endereço do consultório ou da residência, e n° de inscrição do respectivo Conselho profissional.
A prescrição de medicamentos no Brasil é normatizada pelas Leis Federais 5991/ 73 e 9787/99 e pela Resolução nº 357/2001 do Conselho Federal de Farmácia. A prescrição deve ser escrita a tinta, em vernáculo, em letra de forma, clara, por extenso.
A Resolução da Anvisa n° 10/2001 estabelece os critérios que devem ser contemplados na prescrição médica e dispensação de genéricos. No âmbito do SUS, as prescrições pelo profissional responsável adotarão obrigatoriamente a Denominação Comum Brasileira (DCB) ou, na sua falta, a Denominação Comum internacional (DCI). Nos serviços privados de saúde, a prescrição ficará a critério do responsável, podendo ser pelo nome genérico ou comercial, que deverá ressaltar, quando necessária a intercambialidade. No caso do prescritor decidir pela não intercambialidade, essa manifestação deverá ser feita por escrito, de forma clara, legível e inequívoca, não sendo permitido qualquer forma de impressão, colagem de etiquetas, carimbos ou formas automáticas para essa manifestação. <ref> Assistência Farmacêutica na Atenção Básica - Instruções Técnicas para sua Organização. Acesso em 01/11/2019 </ref>
A Prescrição Médica é composta por dados essenciais:
1. Cabeçalho – impresso que inclui nome e endereço do profissional ou da instituição onde trabalha (clínica ou hospital); registro profissional e número de cadastro de pessoa física ou jurídica, podendo conter, ainda, a especialidade do profissional.
2. Superinscrição – constituída por nome e endereço do paciente, idade, quando pertinente, e sem obrigatoriedade do símbolo RX, que significa: “receba”; por vezes, esse último é omitido, e, em seu lugar, se escreve: “uso interno” ou “uso externo”, correspondentes ao emprego de medicamentos por vias enterais ou parenterais, respectivamente.
3. Inscrição – compreende o nome do fármaco, a forma farmacêutica e sua concentração.
4. Subscrição – designa a quantidade total a ser fornecida; para fármacos de uso controlado, essa quantidade deve ser expressa em algarismos arábicos, escritos por extenso, entre parênteses.
5. Adscrição – é composta pelas orientações do profissional para o paciente.
6. Data e assinatura - uma forma de preservar a saúde do paciente, uma vez que a indicação do medicamento deve ser atual, pois a condição clínica do paciente não é estática necessitando, frequentemente, para o seu tratamento, o ajuste na dose dos medicamentos prescritos, assim como, na confirmação da necessidade da continuidade de sua utilização.
Dados Facultativos: Peso, altura, dosagens específicas como usadas na Pediatria. O verso do receituário pode ser utilizado para dar continuidade à prescrição, aprazamento de consulta de controle, e para as orientações de repouso, dietas, possíveis efeitos colaterais ou outras informações referentes ao tratamento.
A dispensação de medicamento também faz parte do processo de atenção à saúde, com foco na prevenção e promoção da saúde, tendo o medicamento como instrumento de ação. Considerando a Resolução nº 357/2001 que aprova o regulamento técnico das Boas Práticas de Farmácia, a presença e atuação do farmacêutico é requisito essencial para a dispensação de medicamentos aos pacientes, cuja atribuição é indelegável, não podendo ser exercida por mandato nem representação e não poderão ser aviadas receitas ilegíveis e/ou que possam induzir a erro ou troca na dispensação dos medicamentos ou que se apresentem em código (sob siglas, números, entre outras).
Tipos de Receitas[editar]
Receita simples-utilizada para a prescrição de medicamentos anódinos (medicamentos de venda livre) e medicamentos de tarja vermelha, com os dizeres “venda sob prescrição médica” – segue as regras descritas na Lei 5.991, de 17 de setembro de 1973.
A validade da receita é de 30 (trinta) dias contados a partir da data de sua emissão para medicamentos a base de substâncias constantes das listas “C1” (outras substâncias sujeitas a controle especial) e “C5” (anabolizantes) do Regulamento Técnico e de suas atualizações. A prescrição poderá conter em cada receita, no máximo 3 (três) substâncias constantes da lista "C1" (outras substâncias sujeitas a controle especial); ou 5 (cinco) substâncias “C4” (anti-retrovirais) deste Regulamento Técnico e de suas atualizações, ou medicamentos que as contenham.
A quantidade prescrita de cada substância constante da lista "C1" (outras substâncias sujeitas a controle especial) e “C5” (anabolizantes), do Regulamento Técnico e de suas atualizações, ou medicamentos que as contenham, ficará limitada a 5 (cinco) ampolas e para as demais formas farmacêuticas, a quantidade para o tratamento correspondente a no máximo 60 (sessenta) dias. No caso de prescrição de substâncias ou medicamentos antiparkinsonianos e anticonvulsivantes, a quantidade ficará limitada até 6 (seis) meses de tratamento. Medicamentos com prescrição contendo quantidades diferentes das mencionadas, o prescritor deverá apresentar justificativa com o CID ou diagnóstico e posologia, datando e assinando as duas vias.
Exemplos Lista C1: Ácido Valproico, Carbamazepina, Etoricoxibe, Lamotrigina e Zolpidem.
Exemplos Lista C5: Nandrolona, Oximetolona e Estanozolol
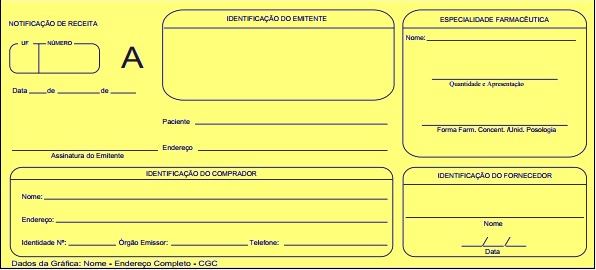
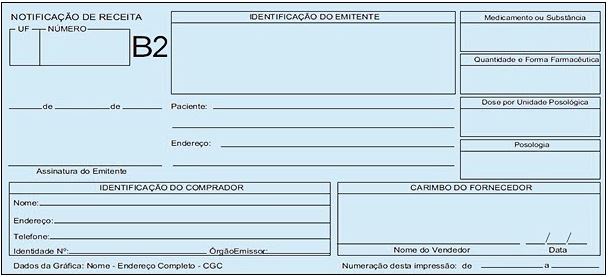
Notificação de receita - Documento padronizado destinado à notificação da prescrição de medicamentos. Autoriza a dispensação de medicamentos a base de substâncias constantes das listas “A1” e “A2” (entorpecentes – cor amarela), “A3”, “B1” e “B2” (psicotrópicas – cor azul), “C2” (retinoicas para uso sistêmico – cor branca) e “C3” (imunossupressoras – cor branca). A Notificação concernente aos dois primeiros grupos (entorpecentes e psicotrópicos) deverá ser firmada por profissional devidamente inscrito no Conselho Regional de Medicina, no Conselho Regional de Medicina Veterinária ou no Conselho Regional de Odontologia; a concernente ao terceiro e quarto grupo (retinoides de uso sistêmico e imunossupressores), exclusivamente por profissional devidamente inscrito no Conselho Regional de Medicina.
Exemplos: Morfina, Oxicodona, Metilfenidato e Lisdexanfetamina
Exemplos: Alprazolam, Clonazepam, Bromazepam e Lorazepam
Exemplos: Sibutramina, Femproporex, Mazindol, Anfepramona
Exemplos: Acitretina, Isotretinoina e Tretinoina.
A Notificação de receita terá validade de 20 (vinte) dias, contados a partir da data de sua emissão e somente dentro da unidade federativa onde foi emitida. A quantidade de Talidomida por prescrição, em cada Notificação de Receita, não poderá ser superior à necessária para o tratamento de 30 (trinta) dias. A prescrição de medicamentos à base de Talidomida deve ser realizada por meio de Notificação de Receita de Talidomida acompanhada do Termo de Responsabilidade/Esclarecimento. Devido aos graves efeitos teratogênicos, o medicamento à base de Talidomida somente poderá ser prescrito para mulheres em idade fértil após avaliação médica com exclusão de gravidez através de método sensível e mediante a comprovação de utilização de, no mínimo, 2 (dois) métodos efetivos de contracepção para mulheres em uso de talidomida (Anexo IV da Resolução 11 de RDC nº 11, de 22 de março de 2011), sendo pelo menos 1 (um) método de barreira. Os pacientes do sexo masculino deverão ser orientados pelo prescritor quanto ao uso de preservativo masculino durante todo o tratamento com Talidomida e após 30 (trinta) dias de seu término. O Termo de Responsabilidade/Esclarecimento obrigatoriamente deverá ser preenchido e assinado pelo prescritor e pelo paciente, em 3 (três) vias, devendo a primeira via permanecer no prontuário, a segunda via ser arquivada na unidade pública dispensadora e a terceira via ser mantida com o paciente. O prescritor deve alertar os pacientes de que o medicamento é pessoal e intransferível e explicar sobre as reações e restrições de uso. <ref> RDC nº 11, de 22 de março de 2011 Acesso em: 04/11/2019 </ref>
Substâncias Antirretrovirais - A prescrição de medicamentos a base de substâncias anti-retrovirais (lista “C4”), só poderá ser feita por médico e será aviada ou dispensada nas farmácias do Sistema Único de Saúde, em formulário próprio estabelecido pelo programa de DST/AIDS, onde a receita ficará retida. Ao paciente, deverá ser entregue um receituário médico com informações sobre seu tratamento. Fica vedada a prescrição de medicamentos a base de substâncias constantes da lista “C4” (antirretrovirais), por médico veterinário ou cirurgiões dentistas. A prescrição de anti-retrovirais poderá conter em cada receita, no máximo 5 (cinco) substâncias constantes da lista "C4" (antirretrovirais) do Regulamento Técnico e de suas atualizações, ou medicamentos que as contenham.
Exemplos: Efavirenz, Lamivudina e Ritonavir
Outras Prescrições[editar]
Antimicrobianos – Segue a RDC 20/2011. A prescrição de medicamentos antimicrobianos deverá ser realizada em receituário privativo do prescritor ou do estabelecimento de saúde, não havendo, portanto modelo de receita específico. A receita deve ser prescrita de forma legível, sem rasuras, em 2 (duas) vias e contendo os seguintes dados obrigatórios: I - identificação do paciente: nome completo, idade e sexo; II - nome do medicamento ou da substância prescrita sob a forma de Denominação Comum Brasileira (DCB), dose ou concentração, forma farmacêutica, posologia e quantidade (em algarismos arábicos ); III - identificação do emitente: nome do profissional com sua inscrição no Conselho Regional ou nome da instituição, endereço completo, telefone, assinatura e marcação gráfica (carimbo); e IV - data da emissão. A receita de antimicrobianos é válida em todo o território nacional, por 10 (dez) dias a contar da data de sua emissão. A receita poderá conter a prescrição de outras categorias de medicamentos desde que não sejam sujeitos a controle especial e não há limitação do número de itens contendo medicamentos antimicrobianos prescritos por receita. A dispensação em farmácias e drogarias públicas e privadas dar-se-á mediante a retenção da 2ª (segunda) via da receita, devendo a 1ª (primeira) via ser devolvida ao paciente <ref> RDC 20/2011 de 5 de maio de 2011 Acesso em 04/11/2019 </ref>.
Considerações[editar]
As prescrições por cirurgiões dentistas e médicos veterinários só poderão ser feitas quando para uso odontológico e veterinário, respectivamente.
Em caso de emergência, poderá ser aviada ou dispensada a receita de medicamento a base de substâncias constantes das listas "C1" (outras substâncias sujeitas a controle especial) em papel não privativo do profissional ou da instituição, contendo obrigatoriamente: o diagnóstico ou CID, a justificativa do caráter emergencial do atendimento, data, inscrição no Conselho Regional e assinatura devidamente identificada. O estabelecimento que aviar ou dispensar a referida receita deverá anotar a identificação do comprador e apresentá-la à Autoridade Sanitária do Estado, Município ou Distrito Federal, dentro de 72 (setenta e duas) horas, para visto <ref> Portaria 344/98 de 12 de maio de 1998 Acesso em 04/11/2019</ref>.
Referências[editar]
<references/>